BIOLOGÍA
FUNCIÓN DE RELACIÓN EN LOS SERES VIVOS
Es la capacidad de los seres vivos de relacionarse con el medio en el que viven. Es una necesidad básica conocer el entorno que los rodea para así poder adaptarse a los cambios que continuamente suceden con el correr del tiempo.
Dicho lo anterior, cabe aclarar que no existe un ser vivo completamente aislado y que no establezca relación con su medio ambiente o con otros seres vivos, pues la relación es vital para su propia supervivencia y para el funcionamiento y equilibrio de los ecosistemas.
La función de relación implica la interacción de las especies con miembros de su mismo grupo social, especie y con otros individuos diferentes a ellos. Un acto de relación puede basarse en el contacto físico o visual y en general, en varios tipos de interacción.
La percepción de estímulos
Los cambios que se producen en el ambiente (estímulos) son percibidos por los seres vivos mediante los receptores sensoriales (células u otras estructuras especializadas).
Existen varios tipos de receptores sensoriales:
- Mecanorreceptores. Detectan estímulos mecánicos, como la presión, contacto, vibraciones, etc.
- Fotorreceptores. Captan estímulos luminosos.
- Quimirreceptores. Captan estímulos químicos, como las sustancias disueltas en el aire o en el agua.
- Termorreceptores. Captan las variaciones de temperatura.
Los estímulos pueden proceder del propio organismo, y son detectados por los propioceptores, un tipo de receptores. Los que proceden del exterior son captados por receptores sensoriales que están agrupados en los órganos de los sentidos. Los principales sentidos de los animales son la vista, la audición, el equilibrio, el olfato, el gusto, el tacto y la detección de temperatura y dolor.
ACTIVIDAD
- consigna en el cuaderno el texto resaltado en el texto anterior
- define en el cuaderno los siguientes conceptos:
- estimulo
- percepción
- relación
- interacción
- individuo
- especie
- videoconferencia lunes 1:00 pm ID: 210-359-9630 Contraseña :cafecito
Las actividades se deben enviar al correo institucional
QUÍMICA
Los símbolos y las formulas químicas a través de la historia
Nomenclatura química
Todos los días, podemos relacionarnos con las personas que nos rodean, gracias a que utilizamos el mismo idioma o lenguaje. De la misma manera, los químicos, sin importar qué idioma hablen en su lugar de origen, necesitan comunicarse entre sí, de manera muy específica. Para ello, han creado un lenguaje propio. Te invitamos a que lo conozcas.
Los símbolos y las fórmulas químicas a través de la historia
El desarrollo de la química como ciencia hizo necesario dar a cada sustancia conocida un nombre que pudiera representarse de forma abreviada, pero que al mismo tiempo incluyera información acerca de la composición molecular de las sustancias y de su naturaleza elemental.
Los alquimistas habían empleado ya símbolos para representar los elementos y compuestos hasta entonces conocidos (figura 1). Muchos de estos símbolos y fórmulas representaban cuerpos celestes, pues, los primeros químicos pensaban que las sustancias materiales estaban íntimamente relacionadas con el cosmos. Dalton fue el primero en utilizar un sistema de signos, desprovisto de misticismo, para los diferentes elementos y con base en estos, para algunos compuestos
Los símbolos modernos para representar los elementos químicos se deben a Berzelius, quien propuso utilizar, en vez de signos arbitrarios, la primera letra del nombre latino del elemento. Cuando varios elementos tuvieran la misma inicial, se representaban añadiendo la segunda letra del nombre. Así, por ejemplo, el carbono, el cobre y el calcio se representan: C, Cu y Ca, respectivamente. Observa que la primera letra del nombre se escribe siempre en mayúscula, mientras que la segunda, cuando está presente, se escribe en minúscula
De la misma manera como estos símbolos representan elementos, las fórmulas indican la composición molecular de las sustancias, mediante la yuxtaposición de los símbolos de los elementos constituyentes. Para indicar el número de átomos presentes de cada elemento integrante de la molécula, se escribe tal cantidad como un subíndice al lado del correspondiente elemento. Por ejemplo, la fórmula del agua H2 O, indica que está constituida por dos átomos de hidrógeno y uno de oxígeno.
Las fórmulas químicas se clasifican en: fórmula empírica, fórmula estructural, fórmula electrónica y fórmula molecular.
La fórmula empírica llamada también fórmula mínima o condensada, indica la relación proporcional entre el número de átomos de cada elemento presentes en la molécula, sin que esta relación señale exactamente la cantidad de átomos. Esta fórmula se puede determinar a partir del porcentaje en peso correspondiente a cada elemento. Por ejemplo, CO2 corresponde a la fórmula empírica o mínima de la glucosa, pero su fórmula molecular es C6 H12O6
La fórmula estructural indica la proporción de átomos y la posición o estructura de la molécula. Por ejemplo, la fórmula para la molécula de agua es
La fórmula electrónica (Lewis) indica los electrones de cada átomo y la unión o enlace que se presenta. Por ejemplo, la fórmula electrónica del cloruro de sodio es
La fórmula molecular muestra con exactitud la relación entre los átomos que forman la molécula. Es múltiplo de la fórmula empírica, por lo tanto, se puede determinar conociendo el peso molecular del compuesto y el peso de la fórmula mínima.
Por ejemplo, si el peso molecular de la glucosa C6 H12O6 es 180 g y el peso de la fórmula mínima CH2 O es de 30 g, entonces,
Como la fórmula mínima es CH2 O, al multiplicarla por 6 da como resultado C6 H12O6 que es la fórmula molecular
ACTIVIDAD
- consigna el el cuaderno la parte resaltada del texto
- escribe en el cuaderno la formula estructural,y electrónica de las siguientes sustancias
a) Óxido mercúrico
b) Ácido fluorhídrico
c) Hidróxido de níquel (II)
d) Sulfato de bario
e) Ácido bórico
f) Carbonato de sodio
Las actividades se deben enviar al correo institucional
Bibliografia
https://www.bioenciclopedia.com/relacion/https://biologia-geologia.com/BG1/652_relacion.htmlcienciasnaturalesmjmdelgado.files.wordpress.com/2018/06/libro-hipertexto-quimica-1.pdf
Chicos el día de mañana se trabajara los mismos temas que esta semana la fecha de entrega de biología es el viernes 15 y de química el jueves 14 de mayo

SEMANA
BIOLOGÍA
Tipos de relación de los seres vivo
Las plantas
las plantas producen unas sustancias llamadas fitohormonas u hormonas vegetales,que tienen la capacidad de activar o inhibir algunas de sus actividades (floración,crecimiento, maduración de frutos entre otros) estas sustancias se producen en algunas partes de las plantas como las hijas y se trasportan por toda la planta generando las respuestas, que se clasifican en dos grupos
Las nastias
son movimientos rápidos y reversibles de algunas partes de la planta que se producen como respuesta a un factor externo.
Hay varios tipos de nastias :
- Fotonastia: la planta responde a la luz, como cuando se abren algunas flores al amanecer o al anochecer o cuando las hojas o las flores se orientan siguiendo el movimiento del Sol.
- Geonastia o gravinastia: respuesta producida por la fuerza de gravedad.
- Tigmonastia: respuesta de por contacto, como por ejemplo, los zarcillos de muchas plantas que permiten que se sujeten a otros lugares.
- Hidronastia: respuesta a la humedad del ambiente, como en la apertura de los esporangios en los helechos.
- Quimionastia: respuesta a sustancias químicas, cambios en el pH, etc.
- Nictinastia: responden a los cambios entre el día y la noche cambiando la posición de las hojas.
- Sismonastia: cuando detectan un golpe o sacudida, como el movimiento de algunas mimosas y de las plantas carnívoras.
- Termonastia: responden a las variaciones de temperatura, como cuando se cierra la flor del tulipán.
- Traumatonastia: respuesta producida como consecuencia de una herida.
TROPISMOS
El término tropismo viene del griego “tropos”, que significa “girar” y tiene que ver con las respuestas de los organismos frente a estímulos externos.
En las plantas, normalmente se dice que los tropismos son el resultado de las respuestas de crecimiento a estímulos específicos como la luz, el tacto, la gravedad, el agua, etc.
Tipos de tropismo
De acuerdo con el tipo de movimiento que inducen, los tropismos pueden clasificarse como positivos o negativos.
Un tropismo positivo es aquel que provoca el movimiento o el crecimiento de una planta o un animal hacia la misma dirección de la que proviene el estímulo que lo dispara; la mayor parte de los movimientos trópicos son positivos y también se conocen como “ortotrópicos”.
Un tropismo negativo, por otra parte, es aquel que induce el movimiento o el crecimiento de un órgano vegetal o de un animal en la dirección contraria al estímulo, es decir, que promueve el crecimiento lejos del estímulo.
Fototropismo y heliotropismo
El fototropismo, como su nombre lo indica, se refiere al movimiento o crecimiento de un organismo en respuesta a estímulos lumínicos. Se observa comúnmente en las plantas y también ha sido comprobado en protozoarios fotosintéticos como los euglénidos, los paramecios y las amebas.
Al igual que todos los tropismos, hay individuos que se mueven o crecen hacia el estímulo y otros que lo hacen “huyendo” de este.
El heliotropismo se refiere, específicamente, al movimiento hacia el sol en respuesta al estímulo lumínico emitido por este; es un término utilizado muy a menudo para describir los movimientos diarios de las hojas que son inducidos por la luz solar.
Geotropismo
El geotropismo, también denominado gravitropismo, es un tipo de movimiento que se da en respuesta a la fuerza de la gravedad. Se dice que todos los órganos vegetales presentan algún tipo de crecimiento o movimiento en una dirección impuesta por la gravedad.
Quimiotropismo
Este es el movimiento o crecimiento de las plantas y de algunos animales en respuesta a estímulos químicos, bien sea atrayentes o repelentes.
Hidrotropismo
Hidrotropismo puede definirse como el crecimiento o el movimiento de un organismo, vegetal o animal, hacia una fuente de agua o alejándose de esta (diferentes potenciales hídricos).
Tigmotropismo
El término tigmotropismo proviene del griego “thigma”, que quiere decir “tocar” y describe las respuestas de crecimiento y/o movimiento de plantas y animales frente a estimulación mecánica o al contacto con un objeto sólido.
ACTIVIDAD
- Define en el cuaderno que es una nastia y que es un tropismo.
- dibuja un ejemplo de cada uno de los tipos de nastias y tropismos.
- Realizar muestreo
Objetivo
observar la reaccion en las plantas
Materiales
- Recipiente
- tierra
- frijoles
- palo de pincho
Procedimiento
sembrar en frijol en el recipiente con tierra, humedecer cada dos días la tierra, cuando ya este una plántula de tamaño pequeño colocar al lado el palo de pincho.
La observación se realizara por 4 semanas, al finalizar se realizara un informe.
Chicos recuerden que esto es semana tres y que no envían la actividad aun, si no a partir de la semana del 18 con plazo limite del 22 de mayo gracias
VALENCIA
Valencia
Se denomina capa de valencia de un átomo a su capa más externa de electrones. Los electrones de esta capa reciben el nombre de electrones de valencia y determinan la capacidad que tienen los átomos para formar enlaces .
Existen dos tipos de valencia:
Valencia iónica: es el número de electrones que un átomo gana o pierde al combinarse con otro átomo mediante un enlace iónico. Así, por ejemplo, cada átomo de calcio pierde dos electrones al formar enlaces iónicos, y por eso la valencia iónica del calcio es dos. Así mismo, cada átomo de oxígeno gana dos electrones al combinarse iónicamente con otro átomo, por lo tanto, su valencia iónica es dos.
Valencia covalente: es el número de electrones que un átomo comparte con otro al combinarse mediante un enlace covalente. Por ejemplo, cada átomo de carbono comparte cuatro electrones al formar enlaces covalentes con otros átomos, y por eso su valencia covalente es cuatro. Algunos elementos poseen más de un número de valencia, lo cual quiere decir que pueden formar más de un compuesto
Número de oxidación
Se conoce como número de oxidación de un elemento a la carga que posee un átomo de dicho elemento, cuando se encuentra en forma de ion.
Los números de oxidación pueden ser positivos o negativos según la tendencia del átomo a perder o ganar electrones. Los elementos metálicos siempre tienen números de oxidación positivos, mientras que los elementos no-metálicos pueden tenerlos positivos o negativos. Similar a lo que ocurre con la valencia, un mismo átomo puede tener uno o varios números de oxidación para formar
Normas para calcular el número de oxidación en compuestos.
En la formulación de un compuesto conviene tener en cuenta las siguientes normas:
Por ejemplo, en la fórmula del óxido de aluminio: Al2 O3 , el aluminio tiene número de oxidación 3+ y el oxígeno 2-, de manera que:
2 (3+) +3 (2-) = 0.
QUÍMICA
VALENCIA
Valencia
Se denomina capa de valencia de un átomo a su capa más externa de electrones. Los electrones de esta capa reciben el nombre de electrones de valencia y determinan la capacidad que tienen los átomos para formar enlaces .
Existen dos tipos de valencia:
Valencia iónica: es el número de electrones que un átomo gana o pierde al combinarse con otro átomo mediante un enlace iónico. Así, por ejemplo, cada átomo de calcio pierde dos electrones al formar enlaces iónicos, y por eso la valencia iónica del calcio es dos. Así mismo, cada átomo de oxígeno gana dos electrones al combinarse iónicamente con otro átomo, por lo tanto, su valencia iónica es dos.
Valencia covalente: es el número de electrones que un átomo comparte con otro al combinarse mediante un enlace covalente. Por ejemplo, cada átomo de carbono comparte cuatro electrones al formar enlaces covalentes con otros átomos, y por eso su valencia covalente es cuatro. Algunos elementos poseen más de un número de valencia, lo cual quiere decir que pueden formar más de un compuesto
Número de oxidación
Se conoce como número de oxidación de un elemento a la carga que posee un átomo de dicho elemento, cuando se encuentra en forma de ion.
Los números de oxidación pueden ser positivos o negativos según la tendencia del átomo a perder o ganar electrones. Los elementos metálicos siempre tienen números de oxidación positivos, mientras que los elementos no-metálicos pueden tenerlos positivos o negativos. Similar a lo que ocurre con la valencia, un mismo átomo puede tener uno o varios números de oxidación para formar
Normas para calcular el número de oxidación en compuestos.
En la formulación de un compuesto conviene tener en cuenta las siguientes normas:
- El número de oxidación de cualquier elemento en estado libre (no combinado) siempre es cero, no importa cuan complicada sea su molécula.
- Un compuesto siempre está formado por unos elementos que actúan con número de oxidación positivo y otros con número de oxidación negativo.
- Al escribir la fórmula del compuesto se coloca primero el o los elementos que actúen con número de oxidación positivo.
- En todo compuesto, la suma algebraica de los números de oxidación de sus elementos multiplicados por los subíndices correspondientes de los mismos, debe ser igual a cero.
Por ejemplo, en la fórmula del óxido de aluminio: Al2 O3 , el aluminio tiene número de oxidación 3+ y el oxígeno 2-, de manera que:
2 (3+) +3 (2-) = 0.
- Cuando todos los subíndices de una fórmula son múltiplos de un mismo número, se pueden dividir entre este número, obteniéndose así la fórmula simplificada del compuesto. Por ejemplo, H2 N2 O6 se debe escribir HNO3 .
- La suma algebraica de los números de oxidación de los elementos en un ion debe ser igual a la carga del ion. Por ejemplo, en el ion carbonato, CO2 3 2, llamamos X al número de oxidación del carbono. Como el oxígeno actúa con número de oxidación 2-, se debe cumplir que ( X+) +3(2-) 5=2- , donde X debe ser igual a 4; así, el carbono actúa con 4+.
ACTIVIDAD
1. El número de oxidación de un elemento se refiere
a la carga que posee un átomo cuando se encuentra como ion. Establece el número de oxidación
del azufre, S, en los siguientes compuestos:
- H2 S
- Na2 SO4
- CaSO3
- CaS
- KHSO3
2 Analiza como se forman los enlaces ionicos y representan gráficamente la formación de los siguientes compuestos:
- litio y cloro,LiCl
- sodio y flúor, NaF
- calcio y oxigeno, CaO
Chicos recuerden que esto es semana tres y que no envían la actividad aun, si no a partir de la semana del 18 con plazo limite del 22 de mayo gracias
Bibliográfia https://www.lifeder.com/tropismo/
SEMANA
QUÍMICA
Función química y grupo funcional
Se llama función química a un conjunto de compuestos o sustancias con
características y comportamiento comunes. Las funciones químicas se
describen a través de la identificación de grupos funcionales que las identifican. Un grupo funcional es un átomo o grupo de átomos que le confieren
a los compuestos pertenecientes a una función química, sus propiedades
principales.
Por ejemplo, la función ácido se reconoce porque en su estructura está
presente el grupo funcional H+ (hidrogenion) y la función hidróxido se
caracteriza por la presencia del grupo funcional OH-(hidroxilo). Así, la
fórmula del ácido clorhídrico es HCl y la del hidróxido de sodio NaOH.
En la química inorgánica las funciones más importantes son: óxido,
ácido, base y sal. A continuación profundizaremos en cada una de ellas,
centrándonos especialmente en los aspectos de nomenclatura de cada
una de las funciones.
Función óxido
Los óxidos son compuestos inorgánicos binarios, es decir, constituidos
por dos elementos, que resultan de la combinación entre el oxígeno y
cualquier otro elemento. Por ejemplo, el cobre arde en presencia del
oxígeno .
Cuando el elemento unido al oxígeno es un metal, el compuesto se llama
óxido básico, mientras que si se trata de un no metal, se le denomina
óxido ácido. Para nombrar este tipo de compuestos basta recordar las
siguientes reglas:
— El oxígeno en la gran mayoría de sus compuestos actúa con número
de oxidación 22.
— En todo compuesto la suma algebraica de los números de oxidación
de sus elementos debe ser igual a cero.
Al nombrar o escribir las fórmulas de los óxidos se pueden presentar
tres situaciones:
Elementos con un único número de oxidación: se incluyen en esta
categoría los elementos de los grupos IA, IIA y IIIA. En este caso para
expresar la fórmula del compuesto basta con escribir los símbolos
de los elementos involucrados dejando un espacio entre ellos para
anotar los subíndices numéricos que permiten equilibrar el número
de cargas positivas y negativas del compuesto de tal manera que se
cumpla la segunda regla.
Elementos que presentan dos números de oxidación: en este caso,
estos elementos pueden combinarse con el oxígeno para dar lugar
a dos tipos de óxidos, con propiedades químicas y físicas propias y
que de igual forma reciben nombres y fórmulas distintos. Dentro de
la nomenclatura tradicional se emplean sufijos (terminaciones) que
permiten diferenciar las dos clases de óxidos. Veamos el siguiente
ejemplo:
₂₂
TALLER
- Define las características de los óxidos
- identifica cual de los siguientes compuestos son óxidos
- ClO
- NaCl
- Fe₂O₃
- HCl
- CaO
BIOLOGÍA
Función de relación
Podemos definir la función de relación como la función que permite al ser humano conocer mejor el medio que le rodea para asegurar así su supervivencia, respondiendo lo mejor posible ante posibles cambios que suceden en su entorno.
Dicho de otra manera, la función de relación es captar los estímulos de nuestro entorno para actuar en función de los mismos.
En la función de relación humana, hay tres elementos básicos para realizar dicha función adecuadamente:
LA VISTA
– El sentido de la vista es el que permite al hombre conocer (ver) el medio que lo rodea y relacionarse con sus semejantes.
– El órgano receptor de ojo globo ocular.
– El ojo cuenta con distintas estructuras que lo protegen: órbita, párpados, glándula lagrimal, pestañas y cejas.
– Los medios transparentes que lo forman son: pupila, cristalino, retina, iris y córnea.
– La visión cambia a medida que las cosas o tu cuerpo se mueven. El cerebro actúa produciendo una serie de
imágenes cientos de veces por segundo, ubicándolas una a continuación
de la otra, como una secuencia.
El cerebro actúa produciendo

EL OÍDO
El sentido del oído nos permite percibir los sonidos, su volumen, tono, timbre y la dirección de la que provienen.
El órgano receptor es el oído
Su estructura se divide en tres partes: oído externo, oído medio y oído interno.
Las vibraciones se transmiten a través del oído medio por una cadena de huesecillos: el martillo, el yunque y el estribo. Al mismo tiempo, originan ondas en el líquido del oído interno. Esos estímulos llegan al cerebro a través los nervios auditivos superiores.
EL GUSTO
– El sentido del gusto consiste en registrar el sabor e identificar determinadas sustancias solubles en la saliva por medio de algunas de sus cualidades químicas.
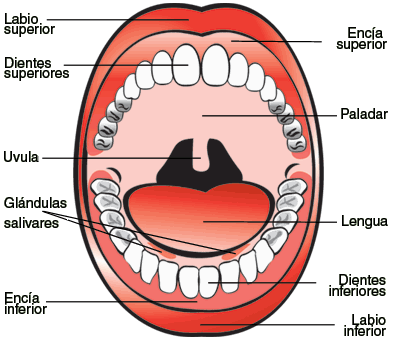
– El órgano receptor del gusto es la boca (en especial la Lengua)
– Sus órganos son los siguientes: papilas gustativas, lengua y paladar.
– Hay cuatro sensaciones gustativas que pueden reconocerse con facilidad: dulce, amargo, ácido ysalado. Cada una depende de corpúsculos gustativos diferentes, que se distribuyen en determinadas zonas de la lengua.
– El sabor dulce se aprecia de preferencia en la punta de la lengua; el amargo en la zona posterior; el ácido en los bordes y el salado en la punta u en los bordes.
– La zona central de la lengua es insensible a los sabores.
EL TACTO
– El sentido del tacto es el encargado de la percepción de los estímulos que incluyen el contacto y la presión, los de temperatura y los de dolor.
– Su órgano sensorial es la piel.
– La mayoría de las sensaciones son percibidas por medio de los corpúsculos, que son receptores que están encerrados en cápsulas de tejido conjuntivo y distribuidos entre las distintas capas de la piel.
– Las capas de la piel se llaman epidermis, dermis, e hipodermis.
EL OLFATO
– El sentido del olfato es el que nos permite discriminar los olores y nos advierte de algunos peligros.
– La nariz es el órgano por el cual penetran todos los olores que sentimos desde el exterior.
– El olfato que está relegado al fondo de la nariz, está constituido por dos cavidades, las fosas nasales, separadas por un tabique.
– La parte interna de la nariz está formada por dos paredes: la pituitaria amarilla y la pituitaria roja o rosada.
EL TACTO
– El sentido del tacto es el encargado de la percepción de los estímulos que incluyen el contacto y la presión, los de temperatura y los de dolor.
– Su órgano sensorial es la piel.
– La mayoría de las sensaciones son percibidas por medio de los corpúsculos, que son receptores que están encerrados en cápsulas de tejido conjuntivo y distribuidos entre las distintas capas de la piel.
– Las capas de la piel se llaman epidermis, dermis, e hipodermis.
TALLER
SEMANA
QUÍMICA
Función química y grupo funcional Se llama función química a un conjunto de compuestos o sustancias con características y comportamiento comunes. Las funciones químicas se describen a través de la identificación de grupos funcionales que las identifican. Un grupo funcional es un átomo o grupo de átomos que le confieren a los compuestos pertenecientes a una función química, sus propiedades principales.
105© Santillana
Componente: Procesos físicos
EJEMPLOS
Por ejemplo, la fu-nción ácido se reconoce porque en su estructura está presente el grupo funcional H1 (hidrogenion) y la función hidróxido se caracteriza por la presencia del grupo funcional OH2 (hidroxilo). Así, la fórmula del ácido clorhídrico es HCl y la del hidróxido de sodio NaOH. En la química inorgánica las funciones más importantes son: óxido, ácido, base y sal. A continuación profundizaremos en cada una de ellas, centrándonos especialmente en los aspectos de nomenclatura de cada una de las funciones.
Función óxido Los óxidos son compuestos inorgánicos binarios, es decir, constituidos por dos elementos, que resultan de la combinación entre el oxígeno y cualquier otro elemento. Por ejemplo, el cobre arde en presencia del oxígeno . Cuando el elemento unido al oxígeno es un metal, el compuesto se llama óxido básico, mientras que si se trata de un no metal, se le denomina óxido ácido. Para nombrar este tipo de compuestos basta recordar las siguientes reglas: — El oxígeno en la gran mayoría de sus compuestos actúa con número de oxidación -2. — En todo compuesto la suma algebraica de los números de oxidación de sus elementos debe ser igual a cero. Al nombrar o escribir las fórmulas de los óxidos se pueden presentar tres situaciones: n Elementos con un único número de oxidación: se incluyen en esta categoría los elementos de los grupos IA, IIA y IIIA. En este caso para expresar la fórmula del compuesto basta con escribir los símbolos de los elementos involucrados dejando un espacio entre ellos para anotar los subíndices numéricos que permiten equilibrar el número de cargas positivas y negativas del compuesto de tal manera que se cumpla la segunda regla . 
TALLER
Define cual de los siguientes óxidos son básicos y cuales ácidos
y coloca su estado de oxidación
BIOLOGÍA
OBJETIVOS
General: Identificar las nastias y los tropismos en las plantas según el ambiente que se presenta
Especifico
Marco teórico: Que son nastias y tropismos
observaciones (con fechas e imágenes )
conclusiones
bibliografia
Este trabajo se debe realizar ha mano en hoja cuadriculada tamaño carta
se debe realizar cita y bibliografía sin dejar renglón buena letra y ortografía.
se debe adelantar el informe, sin llegar a las conclusiones estas se harán al final del experimentos
|




















profe buenos días para cuando es el informe de biología espero que tenga un buen día
ResponderBorrarEste comentario ha sido eliminado por el autor.
ResponderBorrar