BIOLOGÍA
Bases bioquímicas del ADN
ADN es el nombre químico de la molécula que contiene la información genética en todos los seres vivos. La molécula de ADN consiste en dos cadenas que se enrollan entre ellas para formar una estructura de doble hélice. Cada cadena tiene una parte central formada por azúcares (desoxirribosa) y grupos fosfato. Enganchado a cada azúcar hay una de de las siguientes 4 bases: adenina (A), citosina (C), guanina (G), y timina (T). Las dos cadenas se mantienen unidas por enlaces entre las bases; la adenina se enlaza con la timina, y la citosina con la guanina. La secuencia de estas bases a lo largo de la cadena es lo que codifica las instrucciones para formar proteínas y moléculas de ARN.
El ADN, o ácido desoxirribonucleico, es la molécula que contiene la información genética de todos los seres vivos, incluso algunos virus. El nombre viene de su estructura. El ADN tiene una parte central con un azúcar y un fosfato, a la que se enlazan unas moléculas llamadas bases. La desoxirribosa se refiere al azúcar, y el nucleico es el ácido formado por el fosfato y la base nitrogenada. Estas bases pueden ser de 4 tipos: Adenina, citosina, timina y guanina, nombradas normalmente como A, C, T, G. Y el orden en que se combinen una después de la otra, es lo que codifica la información genética. El ADN se organiza estructuralmente en cromosomas. A nivel funcional se organiza en genes, que son piezas de ADN que generan características físicas específicas. Estas características no vienen directamente del propio ADN, sino de una molécula llamada ARN, formada a partir del ADN, y codifica una proteína. Esto es lo que se llama el dogma central de la biología molecular: en el ADN hay genes que generan ARNs mensajeros, y estos generan proteínas. Y esto es lo que da las diferentes características físicas que observamos en individuos, como el color de ojos, o la altura. También se ha visto que algunas veces estas instrucciones estan almacenadas directamente en el ARN, sin necesidad de pasar a proteínas, como en el caso de los micro ARNs. Pero estos suelen ser una excepción.

Por favor ingresar y ver este documento
ACTIVIDAD
- transcribe en el cuaderno el texto resaltado
- dibuja la estructura de ADN con sus partes
- vídeo conferencia lunes 2 Pm
- ID :210-359-9630 contraseña :cafecito
Las actividades se deben enviar al correo institucional
QUÍMICA
Equilibrio en soluciones iónicas
En el siglo XVIII ya se sabía que ciertas soluciones tenían la propiedad de conducir
la electricidad, por lo que más tarde se las llamó soluciones de electrólitos.
A continuación, vamos a considerar algunos de las propiedades de estas soluciones,
deteniéndonos en dos grupos muy especiales: las soluciones ácidas y las
soluciones básicas.
Electrólitos
Un electrólito es una sustancia que se ioniza, es decir, que se disocia, dando
lugar a los iones correspondientes. El resultado es una solución conductora de la
corriente eléctrica. Ejemplos de solución de electrólitos son las soluciones acuosas
de sales, ácidos o bases.
Cuando un soluto no se disocia en iones, sino que por el contrario conserva su
naturaleza molecular, se forma una solución que no conduce la corriente eléctrica.
Este tipo de soluciones se conocen como soluciones moleculares o de no electrólitos.
La mayoría de las sustancias orgánicas, como hidrocarburos y azúcares,
forman soluciones de no electrólitos.
Los electrólitos se dividen teniendo en cuenta un criterio cualitativo en electrólitos
fuertes y electrólitos débiles. Los electrólitos fuertes son compuestos que se
disocian prácticamente en su totalidad, dando lugar a soluciones que conducen
bien la corriente eléctrica. Por el contrario, los electrólitos débiles son sustancias
que se ionizan solo en pequeñas proporciones, con lo cual parte de las moléculas
originales no se disocian y por tanto no contribuyen a la conducción de corrientes
eléctricas, dando origen a soluciones que no conducen adecuadamente la electricidad
Hay tres clases de electrólitos fuertes:
Los ácidos fuertes: son ácidos que forman soluciones acuosas diluidas, en las
cuales cerca del 100% de las moléculas se ionizan. Los más comunes son el
ácido sulfúrico (H2
SO4
), el ácido clorhídrico (HCl), el ácido nítrico (HNO3
),
el ácido bromhídrico (HBr), el ácido perclórico (HClO4
) y el ácido yodhídrico
(HI).
Los ácidos fuertes existen casi exclusivamente como iones en soluciones
acuosas diluidas, como en el siguiente ejemplo:
ac: medio o solución acuosa
n
Las bases fuertes: se forman generalmente con los metales del grupo IA y
algunos del grupo IIA, siendo las más comunes hidróxidos metálicos solubles.
Al igual que los ácidos fuertes, las bases fuertes se caracterizan porque se
ionizan casi completamente en soluciones acuosas diluidas, como se muestra
a continuación para el hidróxido de sodio (NaOH) en solución acuosa:
Las sales solubles: la mayor parte de las sales solubles son compuestos ió-
nicos, tanto en estado sólido como en solución. Por ejemplo, el proceso de
disociación para el cloruro de sodio se puede representar así:
ACTIVIDAD
- Explica:
- ¿Cómo se diferencia un electrólito de otra sustancia?
- ¿Qué diferencias y semejanzas existen entre un electrólito débil y un electrólito fuerte? Justifica tu respuesta
BIBLIOGRAFIA
https://www.genome.gov/es/genetics-glossary/ADN-acido-Desoxirribonucleico
https://cienciasnaturalesmjmdelgado.files.wordpress.com/2018/06/libro-hipertexto-quimica-1.pdf
Chicos el día de mañana se trabajara los mismos temas que esta semana la fecha de entrega de biología es el viernes 15 y de química el jueves 14 de mayo
SEMANA
BIOLOGÍA
Gregor Mendel
(Johann Gregor 8o Gregroio Mendel; Heizendorf, hoy Hyncice, actual República Checa, 1822 - Brünn, hoy Brno, id., 184) Monje y botánico austriaco que formuló las leyes de la herencia biológica que llevan su nombre. Sus rigurosos experimentos sobre los fenómenos de la herencia en las plantas constituyen el punto de partida de la genética, una de las ramas fundamentales y emblemáticas de la biología moderna.
El núcleo de sus trabajos (que comenzó en el año 1856 a partir de experimentos de cruzamientos con guisantes efectuados en el jardín del monasterio) le permitió descubrir las tres leyes de la herencia o leyes de Mendel, gracias a las cuales es posible describir los mecanismos de la herencia y que serían explicadas con posterioridad por el padre de la genética experimental moderna, el biólogo estadounidense Thomas Hunt Morgan (1866-1945).
En el siglo XVIII se había desarrollado ya una serie de importantes estudios acerca de hibridación vegetal, entre los que destacaron los llevados a cabo por Kölreuter, W. Herbert, C. C. Sprengel y A. Knight, y, ya en el siglo XIX, los de Gärtner y Sageret (1825). La culminación de todos estos trabajos corrió a cargo, por un lado, de Ch. Naudin (1815-1899) y, por el otro, de Gregor Mendel, quien llegó más lejos que Naudin.
Las tres leyes descubiertas por Mendel se enuncian como sigue: según la primera, cuando se cruzan dos variedades puras de una misma especie, los descendientes son todos iguales; la segunda afirma que, al cruzar entre sí los híbridos de la segunda generación, los descendientes se dividen en cuatro partes, de las cuales tres heredan el llamado carácter dominante y una el recesivo; por último, la tercera ley concluye que, en el caso de que las dos variedades de partida difieran entre sí en dos o más caracteres, cada uno de ellos se transmite con independencia de los demás.
Para realizar sus trabajos, Mendel no eligió especies, sino razas autofecundas bien establecidas de la especie Pisum sativum. La primera fase del experimento consistió en la obtención (mediante cultivos convencionales previos) de líneas puras constantes y en recoger de manera metódica parte de las semillas producidas por cada planta. A continuación cruzó estas estirpes, dos a dos, mediante la técnica de polinización artificial. De este modo era posible combinar, de dos en dos, variedades distintas que presentan diferencias muy precisas entre sí (semillas lisas-semillas arrugadas; flores blancas-flores coloreadas, etc.).
El análisis de los resultados obtenidos permitió a Mendel concluir que, mediante el cruzamiento de razas que difieren al menos en dos caracteres, pueden crearse nuevas razas estables (combinaciones nuevas homocigóticas). Pese a que remitió sus trabajos con guisantes a la máxima autoridad de su época en temas de biología, W. von Nägeli, sus investigaciones no obtuvieron el reconocimiento hasta el redescubrimiento de las leyes de la herencia por parte de Hugo de Vries, Carl E. Correns y E. Tschernack von Seysenegg, quienes, con más de treinta años de retraso, y después de haber revisado la mayor parte de la literatura existente sobre el particular, atribuyeron a Johan Gregor Mendel la prioridad del descubrimiento.
Las leyes de Mendel
Las leyes mendelianas de la herencia establecen la forma en que se transmiten ciertos caracteres de los seres orgánicos de una generación a otra. Gregor Mendel formuló estas leyes a partir de una serie de experimentos realizados entre 1856 y 1865 que consistieron en cruzar dos variedades de guisantes y estudiar determinados rasgos: el color y la ubicación de las flores en la planta, la forma y el color de las vainas de guisantes, la forma y el color de las semillas y la longitud de los tallos de las plantas.
El método que utilizó Mendel fue transferir el polen (células sexuales masculinas) del estambre (órgano reproductor masculino) de una planta de guisantes al pistilo (órgano reproductor femenino) de una segunda planta de guisantes. Como ejemplo de estos experimentos, supongamos que se recoge el polen de una planta de guisantes con flores rojas y se fecunda con él una planta de guisantes con flores blancas. El objetivo de Mendel era saber de qué color serían las flores de la descendencia de estas dos plantas.
En una segunda serie de experimentos, Mendel estudió los cambios que se producían en la segunda generación. Es decir, supongamos que se cruzan dos descendientes del primer cruzamiento rojo/blanco. ¿Qué color tendrían las flores en esta segunda generación de plantas? Como resultado de sus investigaciones, Mendel definió tres leyes generales sobre la forma en que se transmiten los rasgos de una generación a la siguiente en las plantas de guisantes.
La primera ley de Mendel es denominada ley de los caracteres dominantes o de la uniformidad de los híbridos de la primera generación filial. Si se cruza una línea pura de guisantes de semilla lisa con otra de semilla rugosa, los individuos de la primera generación filial o F1 son todos uniformes; en este caso se parecen todos a uno de los progenitores, el de semilla lisa. El mismo Mendel denominó dominante al carácter que prevalece en el híbrido, y recesivo al que no se manifiesta en él. Posteriormente se vio que la dominancia es un hecho común pero no universal. Muchas veces hay herencia intermedia, porque los híbridos presentan un aspecto intermedio. En otros casos, la situación es de codominancia.
La segunda ley es la ley de la segregación. Si se plantan las semillas de los híbridos de la primera generación filial (F1) y se deja que se autofecunden, se obtiene la segunda generación filial o F2, pudiéndose observar que la proporción entre lisas y rugosas es de 3:1, en el caso de monohibridismo con dominancia. Dicho de otro modo, aparecen en la generación siguiente tres cuartas partes de la descendencia con el carácter dominante (semilla lisa) y una cuarta parte con el carácter recesivo (semilla rugosa). En los casos de monohibridismo con herencia intermedia y de codominancia hay tres tipos de individuos similares a un progenitor, en la proporción de 1:2:1.
ACTIVIDAD
- realiza una historieta donde resuman la biografía de Mendel
- define estos conceptos en el cuaderno
- gen
- genoma
- cromosoma
- dominancia
- recesivo
- genotipo
- fenotipo
- progenie
Chicos recuerden que esto es semana tres y que no envían la actividad aun, si no a partir de la semana del 18 con plazo limite del 22 de mayo gracias
Chicos recuerden que esto es semana tres y que no envían la actividad aun, si no a partir de la semana del 18 con plazo limite del 22 de mayo gracias
QUÍMICA
Conceptos y teorías
sobre ácidos y bases
Los ácidos y las bases fueron reconocidos inicialmente por sus propiedades más
simples, como el sabor: los ácidos tienen un sabor agrio, mientras que las bases
son amargas. Posteriormente, se observó que estas sustancias tenían la capacidad
de cambiar el color de ciertos compuestos, como el papel de tornasol y la fenolftaleína, que, por esta razón, se conocen como indicadores. Los ácidos viran el
papel tornasol de azul a rojo y la fenolftaleína de rojo a incolora, mientras que las
bases viran el papel tornasol de rojo a azul y la fenolftaleína de incolora a rosa.
Como se ha explicado ya, ácidos y bases forman soluciones de electrólitos,
capaces de conducir la electricidad. No obstante, muestran propiedades químicas diferentes. Por ejemplo, los ácidos reaccionan con ciertos metales, como
magnesio, zinc o hierro, produciendo hidrógeno gaseoso. Las bases por su parte
no muestran este comportamiento, al tiempo que son muy buenos detergentes,
presentando una textura jabonosa.
Así mismo, los ácidos y bases reaccionan entre sí dando como resultado una solución compuesta por una sal y agua, que si bien conduce la electricidad, no tiene
las propiedades físico-químicas que tienen ácidos y bases independientemente.
En un intento por dar una explicación al porqué los ácidos y la bases se comportan física y químicamente como lo hacen, se han propuesto una serie de teorías
sobre ellos, llamadas teorías ácido-base. Veamos.
Teoría de Svante Arrhenius
El químico sueco Svante Arrhenius (1859-1927) formuló en 1884 el primer concepto teórico sobre el comportamiento de ácidos y bases, partiendo del efecto
que tienen estas sustancias sobre el agua, cuando se encuentran formando soluciones acuosas. Arrhenius propuso que: un ácido es una sustancia que cuando
se disuelve en agua incrementa la concentración de iones hidrógeno, H+. Mientras
que, una base se define como toda sustancia capaz de incrementar la concentración de iones hidroxilo, OH-, en solución acuosa. La teoría de Arrhenius tenía
algunas limitaciones: se restringía a sustancias en solución acuosa y al definir la
condición ácida y básica a partir de la presencia de iones H1 y OH2, desconocía
una serie de compuestos que, si bien se comportan como ácido o bases, no se
componen de estos iones .
Teoría de Brönsted-Lowry
En 1923, en forma simultánea, pero por separado, los químicos
Johannes Brönsted (1879-1947) y Thomas Lowry (1874-1936) propusieron que las reacciones ácido-base podían ser interpretadas como
transferencias de protones entre los compuestos involucrados. Sobre
esta base, aportaron una definición más amplia de ácidos y bases,
según la cual, un ácido es una especie capaz de ceder uno o más
protones (iones H+), en tanto que una base es una sustancia capaz
de aceptar dichos protones.
De esta manera, cuando un ácido dona un protón, da origen a una
base conjugada, que es una especie capaz de volver a captar el protón
cedido . Igualmente, una base se disocia para dar lugar a un
ion OH-, que es capaz de aceptar un protón, con lo que forma un ácido
conjugado.
Estos conceptos se resumen en las siguientes reacciones esquemáticas:
Ácido Base conjugada → +H +
Base + H+→ Ácido conjugado
En este contexto, una reacción de neutralización se puede representar así:
ácido1 + base2 → base conjugada1 + ácido conjugado2
Veamos dos ejemplos, el primero para la disociación de un ácido, como el ácido cianhídrico y el segundo para un ácido (HCl) y una base (NH3 ) :
Teoría de Lewis
Bajo los conceptos de ácido y base planteados por el químico norteamericano Gilbert Lewis (1875-1946), en 1938, se alcanzó una mayor generalización, que permitió incluir dentro de la definición compuestos que antes no encajaban. Por ejemplo, la reacción entre el dióxido de carbono y el óxido de calcio constituye una interacción ácido-base, desde la teoría de Lewis, que se basa en la donación de pares de electrones en enlaces covalentes.
Estos conceptos se resumen en las siguientes reacciones esquemáticas:
Ácido Base conjugada → +H +
Base + H+→ Ácido conjugado
En este contexto, una reacción de neutralización se puede representar así:
ácido1 + base2 → base conjugada1 + ácido conjugado2
Veamos dos ejemplos, el primero para la disociación de un ácido, como el ácido cianhídrico y el segundo para un ácido (HCl) y una base (NH3 ) :
Teoría de Lewis
Bajo los conceptos de ácido y base planteados por el químico norteamericano Gilbert Lewis (1875-1946), en 1938, se alcanzó una mayor generalización, que permitió incluir dentro de la definición compuestos que antes no encajaban. Por ejemplo, la reacción entre el dióxido de carbono y el óxido de calcio constituye una interacción ácido-base, desde la teoría de Lewis, que se basa en la donación de pares de electrones en enlaces covalentes.
ACTIVIDAD
- Lee y explica cada una de las teorias
a) ¿Cómo se diferencia un electrólito de otra
sustancia?
b) ¿Qué diferencias y semejanzas existen entre un
electrólito débil y un electrólito fuerte?
Justifica
tu respuesta con ejemplos.
3Completa la siguiente tabla con ejemplos.
Chicos recuerden que esto es semana tres y que no envían la actividad aun, si no a partir de la semana del 18 con plazo limite del 22 de mayo gracias
https://www.biografiasyvidas.com/biografia/m/mendel.htm
https://celgado.fileienciasnaturalesmjmds.wordpress.com/2018/06/libro-hipertexto-quimica-1.pdf
https://celgado.fileienciasnaturalesmjmds.wordpress.com/2018/06/libro-hipertexto-quimica-1.pdf
SEMANA
Equilibrio iónico
del agua
En una porción de agua pura, una pequeña parte de las moléculas se presentan disociadas y en equilibrio con las restantes no disociadas, constituyendo lo que se conoce como el equilibrio iónico del agua. Veamos.
Ionización del agua
El agua pura posee una reducida capacidad para conducir la electricidad, por lo que se clasifica como un electrólito débil. Esta propiedad se
debe a la presencia de iones, en muy bajas concentraciones, que sólo
pueden provenir de la ionización de parte de las moléculas de agua.
Durante el proceso de disociación o ionización del agua, algunas moléculas actúan como ácidos y otras como bases, propiciando un intercambio de protones, según el modelo Brönsted-Lowry, como se representa a
continuación:
Soluciones neutras,
ácidas y básicas
BIOLOGÍA
Primera ley de Mendel:
Segregación equitativa (caracteres independientes)
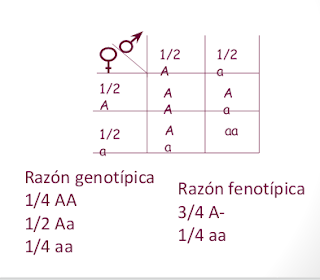
Los dos miembros de un par de alelos segregan en proporciones 1:1. La
mitad de los gametos lleva un alelo y la otra mitad el otro alelo.
Establece que durante la formación de los gametos cada alelo de un par se separa del otro miembro para determinar la constitución genética del gameto filial
Los factores que determinan la herencia se encuentran en dos formas alternativas y cada individuo lleva dos copias (idénticas odistintas), de las cuales una sola se transmite a la descendencia; cada una de esas dos copias tiene la misma probabilidad de pasar a la descendencia, es decir, se transmiten de modo totalmente aleatorio; una de las formas de cada factor domina sobre la otra, de modo que cuando las dos copias son distintas, el carácter se manifiesta como si las dos copias fuesen iguales para la forma dominante.
(Un carácter fenotípico esta controlado por un gen que presenta dos formas alélicas, una dominante y una recesiva).
Por favor ingresar a este link y observar las presentaciones
TALLER
- Define los siguientes conseceptos
- homocigoto
- heterocigoto
- dominancia
- recesivo
2. resuelve el cuestionario de la presentación
Esta actividad se entrega para el 28 y 29 respectivamente
SEMANA
QUÍMICA
Qué es pH:
El pH es una medida de acidez o alcalinidad que indica la cantidad de iones de hidrógeno presentes en una solución o sustancia.
Las siglas pH significan potencial hidrógeno o potencial de hidrogeniones, del latín pondus: peso, potentia: potencia e hydrogenium: hidrógeno, es decir pondus hydrogenii o potentia hydrogenii.
El terminó fue designado por el químico danés Sørense al definirlo como el opuesto del logaritmo en base 10 o el logaritmo negativo de la actividad de los iones de hidrógeno, cuya ecuación es pH= -log10[aH+].
Medición del pH

El pH se puede medir en una solución acuosa utilizando una escala de valor numérico que mide las soluciones ácidas (mayor concentración de iones de hidrógeno) y las alcalinas (base, de menor concentración) de las sustancias.
La escala numérica que mide el pH de las sustancias comprende los número de 0 a 14. Las sustancias más ácidas se acercan al número 0, y las más alcalinas (o básicas) las que se aproximan al número 14. Sin embargo, existen sustancias neutras como el agua o la sangre, cuyo pH está entre de 7 y 7,3.
Las sustancias ácidas como el jugo de limón tiene un pH entre 2 y 3 o la orina entre 4 y 7. Por su parte, los jugos gástricos tienen un valor entre 1 y 2 o los ácidos de baterías que se encuentran entre 1 y 0.
Por el contrario, las sustancias alcalinas o base tiene valores más altos como la leche de magnesia entre 10 y 11 o los limpiadores con amoníaco cuyo valor está entre 11 y 12.
También se pueden calcular las medidas del pH utilizando un potenciómetro o pH Metro, que es un sensor que determina el pH de una sustancia a través de una membrana de vidrio que separa dos soluciones de diferente concentración de protones.
Otra forma de conocer aproximadamente la acidez de una sustancia es utilizando un papel indicador conocido como papel tornasol, que tiene componentes que indican el pH de una sustancia según el cambio de color que sufra el papel.
Vea también:
El pOH
El pOH es el logaritmo negativo en base a 10 de la actividad de los aniones hidróxilo. Tiene las mismas propiedades del pH en disolución acuosa de valor entre 0 y 14, pero en este caso las soluciones con pOH mayores a 7 son ácidas, y básicas o alcalinas las que tengan valores menores de 7.
Se representa con la ecuación pOH = - log[OH-].
Soluciones búfer
Las soluciones búfer, reguladoras o amortiguadoras son utilizadas para mantener el nivel de acidez o alcalinidad de una sustancia durante una reacción química en un período corto, esto con la finalidad de evitar que ocurran otras reacciones químicas no deseadas.
TALLER
Define los siguientes conceptos
- PH
- solución búfer
- POH
Dibuja la escala de PH
VÍDEO DE APOYO
https://drive.google.com/open?id=1DB_7XbsgXEgwRy-gIenr5XHIyLyZbjjg
VÍDEO DE APOYO
https://drive.google.com/open?id=1DB_7XbsgXEgwRy-gIenr5XHIyLyZbjjg
Esta actividad se entrega el 5 junio
https://www.significados.com/ph/
BIOLOGÍA
Realizar la matriz
BIOLOGÍA
Realizar la matriz
- color de ojos
- color de cabello
- color de piel
- cabello lizo o rizado
- color de cabello
Responder las siguientes preguntas
- color de ojos dominantes en la familia
- color de piel dominante
- quien posee mas genes recesivos, padre o madre
- cuales son los tonos dominantes
Esta actividad se entrega el 5 junio
SEMANA 6
RECUERDA LA CLASE POR ZOOM,
TENER APUNTES Y ESTAR PUNTUAL PARA DESARROLLAR LAS ACTIVIDADES.
















Profe osea que el trabajo se manda por el correo institucional??
ResponderBorrarsi señor
ResponderBorrarprofe cual es el trabajo de quimica?
ResponderBorrardame un momento que estoy teniendo problemas con el Internet pero hoy queda en el blog
ResponderBorrarProfe Sigue Sin Aparecer Nada De Química!!
Borrar